Способы получения . 1 . Окисление альдегидов и первичных спиртов - общий способ получения карбоновых кислот. В качестве окислителей применяются />K М n О 4 и K 2 С r 2 О 7 .
2 Другой общий способ - гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода - такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:/>
| ЗNаОН | ||||
| R-CCl 3 | → | R — COOH + Н 2 О | ||
| -3NaCl |
3 . Получение карбоновых кислот из цианидов (нитрилов) - это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия, например:/>
СН 3 -В r + NaCN → CH 3 — CN + NaBr .
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония:
CH 3 CN + 2Н 2 О → CH 3 COONH 4 .
При подкислении раствора выделяется кислота:
CH 3 COONH 4 + HCl → СН 3 СООН + NH 4 Cl .
4 . Использование реактива Гриньяра по схеме:/>
Н 2 О
R
—
MgBr
+ СО 2 →
R
—
COO
—
MgBr
→
R
—
COOH
+
Mg
(OH
)
Br
5 . Гидролиз сложных эфиров:/>
R — COOR 1 + КОН → R — COOK + R ‘ OH ,
R — COOK + HCl → R — COOH + KCl .
6 . Гидролиз ангидридов кислот:/>
(RCO ) 2 O + Н 2 О → 2 RCOOH .
7 . Для отдельных кислот существуют специфические способы получения./>
Муравьиную кислоту получают нагреванием оксида углерода ( II ) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
2С 4 Н 10 + 5 O 2 → 4СН 3 СООН + 2Н 2 О.
Для получения бензойной кислоты можно использовать окисление монозамешенных гомологов бензола кислым раствором перманганата калия:
5С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5С 6 Н 5 СООН + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O .
Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Канниццаро . В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенилметанола (бензилового спирта):
Химические свойства . Карбоновые кислоты - более сильные кислоты, чем спирты, поскольку атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:/>
RCOOH
![]() RCOO — + Н +
RCOO — + Н +
Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты - это, как правило, слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой диссоциации К а = 1,7*10 -5 . />
Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта . Такие заместители, как хлор или фенильный радикал оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект (-/). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, +I. Они понижают кислотность. Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях констант диссоциации K a для ряда кислот. Кроме того, на силу кислоты оказывает влияние наличие сопряженной кратной связи.
|
Карбоновые кислоты Формула K a |
|
Пропионовая CH 3 CH 2 COOH 1,3*10 -5 |
|
Масляная CH 3 CH 2 CH 2 COOH 1,5*10 -5 |
|
Уксусная CH 3 COOH 1,7*10 -5 |
|
Кротоновая CH 3 — CH = CH — COOH 2,0*10 -5 |
|
Винилуксусная CH 2 =CH-CH 2 COOH 3,8*10 -5 |
|
Акриловая CH 2 =CH-COOH 5,6*10 -5 |
|
Муравьиная HCOOH 6,1*10 -4 |
|
Бензойная C 6 H 5 COOH 1,4*10 -4 |
|
Хлоруксусная CH 2 ClCOOH 2,2*10 -3 |
|
Тетроновая CH 3 — C ≡ C — COOH 1,3*10 -3 |
|
Дихлоруксусная CHCl 2 COOH 5,6*10 -2 |
|
Щавелевая HOOC — COOH 5,9*10 -2 |
|
Трихлоруксусная CCl 3 COOH 2,2*10 -1 |
Взаимное влияние атомов в молекулах дикарбоновых кислот приводит к тому, что они являются более сильными, чем одноосновные.
2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот:
2 RCOOH + М g → (RCOO ) 2 Mg + Н 2 ,
2 RCOOH + СаО → (RCOO ) 2 Ca + Н 2 О,
RCOOH + NaOH → RCOONa + Н 2 О,
RCOOH + NaHCO 3 → RCOONa + Н 2 О + СО 2 .
Карбоновые кислоты - слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей:
CH 3 COONa + HCl → СН 3 СООН + NaCl .
Соли карбоновых кислот в водных растворах гидролизованы:
СН 3 СООК + Н 2 О
![]() СН 3 СООН + КОН.
СН 3 СООН + КОН.
Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных.
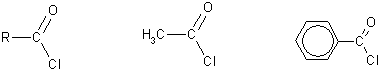
3 . Образование функциональных производных карбоновых кислот. При замещении группы ОН в карбоновых кислотах различными группами (/>X ) образуются функциональные производные кислот, имеющие общую формулу R -СО- X ; здесь R означает алкильную либо арильную группу. Хотя нитрилы имеют другую общую формулу ( R - CN ), обычно их также рассматривают как производные карбоновых кислот, поскольку они могут быть получены из этих кислот.
Хлорангидриды получают действием хлорида фосфора ( V ) на кислоты:
R-CO-OH + РС l 5 → R-CO-Cl + РОС l 3 + HCl .
|
Соединение примеры |
|
Кислота
Этановая(уксусная) Бензойная кислота хлорангидрит кислоты
Этаноилхлорид Бензоилхлорид (ацетилхлорид) ангидрид кислоты
Этановый(уксусный) бензойный ангидрит Ангидрит сложый эфир
Этилэтаноат(этилацетат) Метилбензоат амид Этанамид(ацетамид) Бензамид Нитрил Этаннитрил Бензонитрил (ацетонитрил) |
Ангидриды образуются из карбоновых кислот при действии водоотнимающих средств:
2 R — CO — OH + Р 2 О 5 → (R — CO -) 2 O + 2НРО 3 .
Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации):
Механизм реакции этерификации был установлен методом "меченых атомов".
Сложные эфиры можно также получить при взаимодействии хлорангидридов кислот и алкоголятов щелочных металлов:
R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl .
Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов :
СН 3 -СО-С l + CН 3 → СН 3 -СО-CН 2 + HCl .
Кроме того, амиды могут быть получены при нагревании аммонийных солей карбоновых кислот:
При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов :
| Р 2 0 5 | ||
| CH 3 — CO — NH 2 |
→ |
CH 3 — C ≡ N + Н 2 О |
Функциональные производные низших кислот — летучие жидкости. Все они легко гидролизуются с образованием исходной кислоты:
R-CO-X + Н 2 О →R-CO-OH + НХ .
В кислой среде эти реакции могут быть обратимы. Гидролиз в щелочной среде необратим и приводит к образованию солей карбоновых кислот, например:
R-CO-OR ‘ + NaOH → R-CO-ONa + R’OH.
4 . Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода (а-атоме):/>
| р кр | ||
|
СН 3 -СН 2 -СООН + Вr 2 |
→ |
СН 3 -СНВr-СООН + НВr |
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН,
СН 2 =СН-СООН + С l 2 → СН 2 С l -СНС l -СООН,
СН 2 =СН-СООН + HCl → СН 2 С l -СН 2 -СООН,
СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН,
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации .

5 . Окислительно-восстановительные реакции карбоновых кислот./>
Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды:
Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:

Муравьиная кислота - сильный восстановитель и легко окисляется до СО 2 . Она дает реакцию "серебряного зеркала" :
НСООН + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
или в упрощенном виде:
C Н 3 НСООН + Аg 2 О → 2Аg + СО 2 + Н 2 О.
Кроме того, муравьиная кислота окисляется хлором:
НСООН + Сl 2 → СО 2 + 2 HCl .
В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О:
СН 3 СООН + 2О 2 → 2СО 2 + 2Н 2 О.
6 . Реакции декарбоксширования . Насыщенные незамещенные монокарбоновые кислоты из-за большой прочности связи С-С при нагревании декарбоксилируются с трудом. Для этого необходимо сплавление соли щелочного металла карбоновой кислоты со щелочью:/>
Появление электронодонорных заместителей в углеводородном радикале способствует реакции декарбоксилирования :
Двухосновные карбоновые кислоты легко отщепляют СО 2 при нагревании:
Органические соединения с карбоксильной группой CООH часто встречаются в природе и быту. Без их производных мы не может выжить, а без всем известного уксуса не представляем себе жизни. Без них невозможно получить многих веществ, к которым мы привыкли в быту. Какие химические свойства карбоновых кислот, какие их виды существуют в природе, как их получить, где они применяются и с какими веществами реагируют, рассмотрим в этой статье.
Все они имеют кислые свойства, потому что эта группа легко отщепляет протон. Вещества содержат углеводородный радикал. По нему и называется соединение: например - CH 3 – CH 2 – COOH - пропановая. Формула карбоновых кислот - R – СООН, где R - это углеводородный радикал.
Общая формула
В зависимости от углеводородного радикала, который связывается с карбоксильной группой, существует такая классификация этих веществ:
- Ароматические. Они имеют ароматический радикал, простейшая из них - бензойная.
- Алифатические (все соединения, не содержащие ароматической группы), в том числе ациклические (с открытой цепью) и замкнутые. Существуют предельные карбоновые кислоты (насыщенные) и непредельные (ненасыщенные, имеющие двойные и тройные связи). К ним относят уксусную, капроновую и др.
- Алициклические содержат замкнутые кольца атомов углерода с разной степенью насыщенности.
- Гетероциклические. В них наряду с углеродом входят атомы других элементов.
Существует классификация карбоновых кислот по количеству атомов углерода: одноосновные, двухосновные и многоосновные.
Названия
Все названия соединений с карбоксильной группой образуются по наименованию углеводорода, например:
- метановая (от углеводорода метана СН 4 образовалась кислота НСООН - метановая);
- этановая - СН 3 COOH;
- пропановая - С 2 Н 5 COOH;
- 2-этилбутановая - CH 3 – CH 2 – CH – CH 2 – CH 3 СOOH.
Но некоторые кислотные соединения имеют исторические, то есть тривиальные названия:
- муравьиная - HCOOH;
- уксусная - CH 3 COOH;
- пропионовая - C 2 H 5 СООН;
- масляная - С 3 Н 7 СOOH;
- капроновая - С 6 Н 13 COOH;
- стеариновая - С 17 Н 35 СOOH;
- CH 2 =CH — CОOH - акриловая;
- СH 3 - (CH 2) 7 - CH=CН - (CH 2)7 - COOН - олеиновая;
- HООC - CООH - щавелевая.
Необходимо помнить, что такоеназвание употребляется наряду с основным.

Названия
Физические свойства
При знакомстве с классом карбоновые кислоты физические свойстваэтих веществ очень важны.
- Одноосновные кислоты имеют намного более высокую температуру плавления и кипения, чем у соответствующих углеводородов и спиртов. Так, температура плавления НСООН немногим выше 8 градусов, а кипения - более 100 градусов. Разветвленные изомеры имеют температуру плавления ниже.
- Хорошая растворимость в воде. С увеличением числа атомов углерода этот показатель снижается: так, в 100 г воды растворяется всего лишь 15 мг С 9 Н 19 СООН. Все кислотные соединения с углеродным числом более 10 практически не растворяются в воде.
- Низшие соединения являют собой подвижные легкие жидкости с резким запахом; бутановая (масляная) кислота имеет запах горького масла.
- Вещества из рассматриваемого класса с количеством атомов С от 4 до 9 - маслянистые.
- Соединения с большим количеством атомов С - твердые.
Применяя карбоновые кислоты, физические свойстваих нужно учитывать в работе.

Физические свойства
Химические свойства
Химические свойства карбоновых кислот такие же, что и у неорганических;
- Диссоциация в воде. Образуется ион водорода и карбоксилат ион. Наиболее сильной является метановая. Другие соединения имеют среднюю силу. Она уменьшается по мере роста атомов С.
- Реакция с металлами: 2НСООН + → ()2 + 2.
- Реакция с щелочами: → 3 + 2.
- Реакция с основным оксидом: 2НСООН +СаО → ()2 + 2.
- Реакция с солями слабых кислот: 2СН 3 СН + 23 → 23 + 23. В этом случае образуется натрия ацетат, а 23 выпадает в осадок.
- Реакция с аммиаком: С 2 Н 5 СООН + 3 → 254. В этом случае образуется пропионат аммония.
- Взаимодействие со спиртами: СН 3 СН + С 2 Н 5 ОН → СН 3 СС 2 Н 5 + Н 2 О.
- Вступают в реакции с галогенами с синтезом хлопроизводных карбоновой кислоты и хлористого водорода. Эта реакция происходит вместе с катализатором - красного фосфора. При окислении хлором НСООН разлагается до углекислого газа и хлористого водорода.
- При воздействии чистого кислорода уксус окисляется до углекислого газа и воды.
Полезное видео: карбоновые кислоты - строение, номенклатура, изомерия
Нахождение в природе
Все рассматриваемые вещества содержатся в природе. Организмы живых существ постоянно контактируют с кислотными соединениями..
Предельные карбоновые кислотыможно обнаружить в таком виде:
- Муравьиная находится в крапиве, яде пчел, выделениях муравья.
- Уксусная образуется во время уксусно-кислого брожения.
- Валериановая находится в корнях валерианы.
- Капроновая содержится в молоке коз.
- Миристиновая содержится в приятно пахнущих частях мускатного ореха.
- Пальмитиновая в значительном количестве содержится в пальмовом масле.
- Стеариновая - основа свиного сала. Относится к очень важным жирным кислотным соединениям.
- Церотиновая имеет большое количество атомов С и есть в восках.
Интересно! Кислый вкус испортившегося вина объясняется как раз наличием в нем уксуса. А неприятный запах испорченного масла объясняется тем, что в нем в большом количестве находится неприятно пахнущая С 3 Н 7 СООН.
В природе также распространены и двухосновные карбоновые кислотные соединения:
- Кислый вкус щавеля и ревеня объясняется нахождением в нем щавлевой кислоты. Она образуется при разложении некоторых аминокислот. В человеческом организме при некоторых обменных заболеваниях может образовываться нерастворимая кальциевая соль этого вещества.
- При прокаливании янтаря образуется янтарная кислота.
- Малоновая содержится в яблоках.
- Глутаровая содержится в клейковине злаковых. Отсюда она получила свое название.
Названий очень много, и по мере развития науки их количество увеличивается.
Интересно ! Гидроксикислоты синтезируются при молочнокислом сбраживании углеводов. Привычное всем скисание молока с образованием простокваши и кефира - это не что иное, как естественный синтез молочной кислоты. Тот же процесс происходит при естественном брожении вина или пива.

Нахождение в природе
Как получить
Получение рассматриваемых веществ в промышленности имеет много способов.
Рассмотрим некоторые их них:
- Выделение из природных материалов - жиров, масел и восков.
- Окисление насыщенных углеводородов. П роисходит при повышенной температуре, например: 2СН 4 + 3О 2 → 2 + 22.
- Окисление углеводородов с двойной связью, например = + О 2 - СН 3 СОО.
- Бензойную можно получить таким путем: 565-CH 3 + 6КМnO4 + 9H 2 SO 4 → 5C 6 H 5 — + 3К 2 SO 4 + 6МnSO 4 + 14H2O.
- Муравьиную можно синтезировать с помощью таких реакций: CO + NаOH → НCOON и HCООNа + H 2 SO 4 → HCOOH + .
В условиях лаборатории рассматриваемые соединения можно получить с помощью таких реакций:
- Применение солей: R – COONa + HCl → R – COOH + NaCl.
- Растворение соответствующих ангидридов в воде: (R – CO)2O + H 2 O → 2 R – COOH. Так можно получить, например, карбоновую кислоту С 2 Н 5 ССОН.
- Окисление альдегидов: R – COH + [O] → R – COOH.
- Окисление спиртов: R – CH 2 – OH + 2[O] → R – COOH + H 2 O.
- С применением цианида: СH 3 – Вr + Na – C≡N → CH 3 – CN + NaВr .
Во всех случаях символ R означает любой углеводородный радикал.

Применение органических соединений
Применение карбоновых кислотшироко распространено в промышленности и быту. Так, НСООН обладает выраженными антибактериальными свойствами. Применяется для изготовления клеев, лаков, красителей. Сложные эфиры вещества - это растворители для пахнущих веществ.
Интересно! НСООН применяется в пищевой промышленности как пищевая добавка с кодом Е236. Добавка содержится как консервант в кондитерских и консервированных, некоторых молочных продуктах. Без нее невозможно нормально продезинфицировать пивные и винные бочки.
Известный всем муравьиный спирт применяется в медицине в качестве противовоспалительного, болеутоляющего средства. Рефлекторно действует как раздражитель. НСООН используется для повышения срока хранения сена, силоса, потому что это вещество замедляет процесс гниения и распада органических веществ.
Уксус находит широкое применение не только как добавка к пище и для приготовления консервов. С ее помощью можно легко синтезировать лаки, красители для тканей. Огромные количества СН 3 СООН расходуются для выработки широко используемого ацетатного волокна, пластмассы, кинопленки, устойчивой к воспламенению и возгоранию, ядов, органического стекла. Ацетаты широко используются в сельском хозяйстве как эффективные ядохимикаты.
Несмотря на отвратительный запах прогорклого масла, С 3 Н7СООН используется для терапии патологий пищеварительного тракта. Она регулирует кишечную перистальтику, способствует развитию полезных бактерий. Сложные эфиры этого вещества имеют приятный запах, а поэтому они применяются в качестве основы для парфюмерной композиции.
Стеарин и пальмитин используют в процессе реакций с глицерином и образует мыло. Косметические вещества быстро впитываются и не вызывают аллергии. В химии применяют одноосновные карбоновые кислоты с более высоким углеродным числом.
Щавелевая применяется почти во всех отраслях промышленности благодаря ее уникальным свойствам.
Полезное видео: карбоновые кислоты и их соли
Вывод
Вещества с карбоксильной группой широко распространены в природе. Благодаря своим свойствам они широко применяются в быту и в промышленности. Количество этих соединение все время возрастает по мере развития химической науки.
Вконтакте
Карбоновые кислоты (2 лекции)
1. Определение. Классификация.
2. Изомерия и номенклатура одноосновных карбоновых кислот
3. Физические свойства кислот
4. Химические свойства. Строение карбонильной группы.
Карбоновые кислоты – это производные углеводородов, содержащие карбоксильную группу (-СООН).
Классификация карбоновых кислот
Карбоновые кислоты классифицируют по двум структурным признакам.
1) По числу карбоксильных групп кислоты подразделяются на:
Ø одноосновные (монокарбоновые)
Ø многоосновные (дикарбоновые, трикарбоновые и т. д.)
. 
2) По характеру углеводородного радикала различают кислоты:
Ø предельные (например, CH3CH2CH2COOH)
Ø непредельные (CH2=CHCH2COOH)
Ø ароматические (RC6H4COOH)
Одноосновные предельные карбоновые кислоты
Общая формула таких кислот – CnH2nO2 или CnH2n+1COOH
Номенклатура и изомерия карбоновых кислот
Кислоты с числом углеродных атомов меньше четырех не имеют изомеров. Если число атомов равно четырем, кислоты имеют два изомера, если число атомов равно пяти – пять изомеров.
Для названия кислот используются следующие типы номенклатуры:
ü тривиальная
ü рациональная.
Названия карбоновых кислот строятся с использованием в качестве основы названия уксусной кислоты. Остальные кислоты рассматриваются как ее производные с замещением атомов водорода в метильной группе на более сложные радикалы. Остальные правила полностью соответствуют правилам рациональной номенклатуры для углеводородов (подробно они изложены в начале лекционного курса).
При составлении названия карбоновой кислоты за основу берут наиболее длинную цепь, включающую карбоксильную группу. Нумерацию начинают с атома углерода карбоксильной группы (цифру, указывающую на положение функциональной группы, не ставят). К названию углеводорода по числу атомов углерода в главной цепи прибавляют суффикс –овая кислота . Цифрами и приставками указывают положение и число заместителей.
Номенклатура карбоновых кислот идентична номенклатуре альдегидов. что значительно облегчает ее понимание и изучение.
Названия отдельных представителей карбоновых кислот
Тривиальное название | Рациональное | ||
муравьиная | муравьиная | метановая |
|
уксусная | уксусная | этановая |
|
СН3-СН2-СООН | пропионовая | метилуксусная | пропановая |
СН3-СН2-СН2-СООН | масляная | этилуксусная | бутановая |
СН3-СН2-СН2-СН2-СООН | валерьяновая | пропилуксусная | пентановая |
| метилвторбутил-уксусная | 2,3-диметил-пентановая |
Получение карбоновых кислот
Многие способы получения одноосновных кислот были рассмотрены в предыдущих лекциях:
1) окисление спиртов
2) озонолиз алкенов
3) окисление карбонильных соединений (альдегидов и кетонов)
4) гидролиз геминальных тригалогенпроизводных углеводородов (аналогичен гидролизу дигалогенпроизводных в получении альдегидов, способ 5):

5) гидролиз производных кислот (галогенпроизводных, сложных эфиров, нитрилов)

6) карбоксилирование металлоорганических соединений
Это универсальный способ получения карбоновых кислот, является лабораторным методом.

Физические свойства
Низшие кислоты с числом атомов С1-С3 – бесцветные жидкости, с характерным острым запахом.
Кислоты состава С4-С9 – это маслянистые жидкости с неприятным запахом, плохо растворимые в воде.
Кислоты состава С10 и выше – твердые вещества не растворимые в воде.
Таким образом, с увеличением молекулярной массы растворимость кислот в воде уменьшается.
Высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей, с этим связана и хорошая растворимость в воде (происходит образование водородных связей с молекулами воды).
https://pandia.ru/text/78/506/images/image008_0.gif" alt="990 байт" width="195" height="91 src=">
Химические свойства кислот
Строение карбоксильной группы
Карбоксильная группа сочетает в себе две функциональные группы - карбонил и гидроксил, взаимно влияющие друг на друга:

Кислотные свойства карбоновых кислот выражены достаточно ярко. Это объясняется взаимным влиянием атомов в карбоксильной группе. Электронная плотность в которой смещена на более электроотрицательному кислороду гидроксигруппы, что ослабляет связь О-Н и облегчает отделение атома водорода, т. е.облегчает диссоциацию кислоты (это обусловлено тем, что +М-эффект ОН-группы преобладает перед –I-эффектом). Подвижность протонов расположенных в α-положении также определяется строением СООН-группы (подробные объяснения изложены в лекции «Альдегиды и кетоны»).
1) Кислотные свойства
Диссоциация кислот. В водном растворе карбоновые кислоты распадаются на ионы и обладают кислой реакцией. Это можно обнаружить с помощью индикатора, что считается качественным определением кислот . Например, лакмус приобретает красный цвет.
https://pandia.ru/text/78/506/images/image011_0.gif" width="476 height=87" height="87">
граничные резонансные структуры связи С-О выравниваются
Мезомерия – это явление выравнивания электронной плотности между двумя атомами кислорода.
Карбоновые кислоты более сильные кислоты, чем спирты.
Муравьиная кислота – самая сильная, это связано с отсутствием электронодонорного эффекта алкильных групп. Заместители с положительным индуктивным эффектом (электронодонорные – СН3, С2Н5) понижают кислотность, оторвать водород от кислорода в ОН-группе сложнее.
Образование солей . Кислоты способны образовывать соли с металлами, их оксидами и гидроксидами.
а) при взаимодействии с металлами:
2RCOOH + Mg ® (RCOO)2Mg + H2
б) в реакциях с гидроксидами металлов:
2RCOOH + NaOH ® RCOONa + H2O
2) Реакции по ОН-группе
Образование сложных эфиров (R"–COOR") – реакция этерификации. Это реакция взаимодействия кислот со спиртами в присутствии минеральных кислот. Реакция обратима.
уксусная кислота этиловый спирт этиловый эфир уксусной кислоты
Кислоты линейного строения, типа R-CH2-COOH скорее вступают в реакцию, чем кислоты разветвленного строения:R2CH-COOH, R3C-COOH. Роль катализатора в реакции этерификации играют ионы Н+:

Реакция протекает по следующему механизму: кислород карбонильной группы захватывает протон и образует карбкатион I . Этот карбкатион присоединяет молекулу спирта за счет неподеленной пары атома кислорода с образованием комплекса II . Комплекс II способен обратимым образом распадаться и образовывать карбкатион III , при диссоциации которого образуется сложный эфир (катализатор – протон при этом освобождается).
Большой интерес в этой реакции представлял вопрос: кислота или спирт отщепляют гидроксил в реакции эфирообразования. С помощью «меченых атомов» (тяжелого изотопа 18О) было показано, что вода образуется за счет водорода спирта и гидроксила кислоты.

(если меченый кислород находится в спирте, то образующаяся вода содержит обычный кислород)
Реакции с полным замещением ОН-группы.
Получение производных карбоновых кислот.
1) галогенангидриды кислот можно получить действием пентахлорида фосфора (PCl5), хлористого тионила (SOCl2).

2) галоген в галогенангидридах обладает большой реакционной способностью, поэтому галогенангидриды используют в качестве ацилирующих средств. Так получают ангидриды кислот.

Например, уксусный ангидрид (R= CH3) используется в органическом синтезе как сильное водоотнимающее средство.
3) образование амидов осуществляется действием аммиака .
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами. При участии щелочей гидролиз жиров происходит необратимо. Продуктами в этом случае являются мыла - соли высших карбоновых кислот и щелочных металлов.
https://pandia.ru/text/78/506/images/image023_0.gif" width="103" height="53">
Акриловая кислота поучается синтетическим способом. Представляет собой жидкость с резким запахом. Легко полимеризуется с образованием полиакриловой кислоты.
Значительное практическое значение имеют эфиры акриловой кислоты, а точнее продукты их полимеризации:

этиловый эфир акриловой кислоты
Полиакрилаты прозрачны и применяются для изготовления различных пластмасс и органического стекла. Большей твердостью по сравнению с полиакрилатами обладают метакрилаты – эфиры метакриловой кислоты.
Лучшим органическим стеклом является плексиглас – метиловый эфир полиметакриловой кислоты. Плексиглас применяется в медицине для изготовления протезов.

метиловый эфир метакриловой кислоты
В целом для непредельных кислот характерны многие реакции, характерные для алкенов: присоединение галогенов, водорода по кратной связи, окисление перманганатом калия, диеновый синтез.
Двухосновные карбоновые кислоты.
Простейшая двухосновная кислота – щавелевая (впервые была найдена в щавеле) или этандиовая кислота. Следующий представитель – малоновая или пропандиовая кислота. Двухосновная кислота с четырьмя атомами углерода называется янтарной или бутандиовой.
Важнейшие реакции таких кислот – получение конденсационных полимеров.
Реакции этерификации и получения амидов дикарбоновых кислот лежат в основе промышленного производства исключительно важных в практическом отношении конденсационных полимеров.
Конденсация дикарбоновой кислоты и алкандиола ведет к образованию полиэфира. Полиэфиры широко используют в производстве синтетических волокон.
Один из наиболее важных полиэфиров – лавсан – получают поликонденсацией терефталевой кислоты и этиленгликоля.

Конденсация дикарбоновой кислоты с диамином ведет к образованию полиамида . Полиамиды служат для получения синтетических материалов (синтетическая шерсть ). Важный в практическом отношении полиамид – найлон-6,6 – получают поликонденсацией адипиновой кислоты и гексаметилендиамина.

В развернутом виде это выглядит следующим образом:

В названии «найлон-6,6» первая цифра указывает на число атомов углерода в дикарбоновой кислоте, а вторая – число углеродных атомов в диамине.
Если процессу поликонденсации подвергают смесь ароматической дикарбоновой кислоты (например, терефталевой кислоты) и ароматического диамина, то получают полиамидные материалы, сравнимые по прочности с изделиями из стали:
Карбоновыми кислотами называют соединения, в которых содержится карбоксильная группа:
Карбоновые кислоты различают:
- одноосновные карбоновые кислоты;
- двухосновные (дикарбоновые) кислоты (2 группы СООН ).
В зависимости от строения карбоновые кислоты различают:
- алифатические;
- алициклические;
- ароматические.
Примеры карбоновых кислот.


Получение карбоновых кислот.
1. Окисление первичных спиртов перманганатом калия и дихроматом калия:

2. Гибролиз галогензамещенных углеводородов, содержащих 3 атома галогена у одного атома углерода:
3. Получение карбоновых кислот из цианидов:
При нагревании нитрил гидролизуется с образованием ацетата аммония:
При подкисления которого выпадает кислота:
4. Использование реактивов Гриньяра:
5. Гидролиз сложных эфиров:
6. Гидролиз ангидридов кислот:
7. Специфические способы получения карбоновых кислот:
Муравьиная кислота получается при нагревании оксида углерода (II) с порошкообразным гидроксидом натрия под давлением:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
Бензойную кислоту получают окислением монозамещенных гомологов раствором перманганата калия:
Реакция Каннициаро . Бензальдегид обрабатывают 40-60% раствором гидроксида натрия при комнатной температуре.

Химические свойства карбоновых кислот.
В водном растворе карбоновые кислоты диссоциируют:

Равновесие сдвинуто сильно влево, т.к. карбоновые кислоты являются слабыми.
Заместители влияют на кислотность вследствие индуктивного эффекта. Такие заместители оттягивают электронную плотность на себя и на них возникает отрицательный индуктивный эффект (-I). Оттягивание электронной плотности приводит к повышению кислотности кислоты. Электронодонорные заместители создают положительный индуктивный заряд.

1. Образование солей. Реагирование с основными оксидами, солями слабых кислот и активными металлами:

Карбоновые кислоты - слабые, т.к. минеральные кислоты вытесняют их из соответствующих солей:
2. Образование функциональных производных карбоновых кислот:
3. Сложные эфиры при нагревании кислоты со спиртом в присутствие серной кислоты - реакция этерификации:
4. Образование амидов, нитрилов:
3. Свойства кислот обуславливаются наличием углеводородного радикала. Если протекает реакция в присутствие красного фосфора, то образует следующий продукт:
4. Реакция присоединения.

8. Декарбоксилирование. Реакцию проводят сплавлением щелочи с солью щелочного металла карбоновой кислоты:
9. Двухосновная кислота легко отщепляет СО 2
при нагревании:
Дополнительные материалы по теме: Карбоновые кислоты.
Калькуляторы по химии |
|
| Химия онлайн на нашем сайте для решения задач и уравнений. | |
В табл. 19.10 указаны некоторые органические соединения, относящиеся к карбоновым кислотам. Характерный признак карбоновых кислот - наличие в них карбоксильной
Таблица 19.10. Карбоновые кислоты
(см. скан)
функциональной группы. Карбоксильная группа состоит из карбонильной группы, связанной с гидроксильной группой. Органические кислоты с одной карбоксильной группой называются монокарбоновыми кислотами. Их систематические названия имеют суффикс -ов(ая). Органические кислоты с двумя карбоксильными группами называются дикарбоновыми кислотами. Их систематические названия имеют суффикс -диов(ая).
Насыщенные алифатические монокарбоновые кислоты образуют гомологический ряд, который характеризуется общей формулой . Ненасыщенные алифатические дикарбоновые кислоты могут существовать в форме различных геометрических изомеров (см. разд. 17.2).
Физические свойства
Низшие члены гомологического ряда насыщенных монокарбоновых кислот при нормальных условиях представляют собой жидкости, обладающие характерным острым запахом. Например, этановая (уксусная) кислота имеет характерный «уксусный» запах. Безводная уксусная кислота при комнатной температуре представляет собой жидкость. Она замерзает при превращаясь в льдистое вещество, которое называется ледяной уксусной кислотой.
Все дикарбоновые кислоты, указанные в табл. 19.10, при комнатной температуре представляют собой белые кристаллические вещества. Низшие члены рядов монокарбоновых и дикарбоновых кислот растворимы в воде. Растворимость карбоновых Кислот уменьшается по мере возрастания их относительной молекулярной массы.
В жидком состоянии и в неводных растворах молекулы монокарбоновых кислот димеризуются в результате образования между ними водородных связей:

Водородная связь в карбоновых кислотах сильнее, чем в спиртах. Это объясняется высокой полярностью карбоксильной группы, обусловленной оттягиванием электронов от атома водорода по направлению к карбонильному атому кислорода:

Вследствие этого карбоновые кислоты имеют сравнительно высокие температуры кипения (табл. 19.11).
Таблица 19.11. Температуры кипения уксусной кислоты и спиртов с близкими значениями относительной молекулярной массы

Лабораторные методы получения
Монокарбоновые кислоты можно получать из первичных спиртов и альдегидов окислением с помощью подкисленного раствора бихромата калия, взятого в избыточном количестве:
Монокарбоновые кислоты и их соли можно получать гидролизом нитрилов либо амидов:

Получение карбоновых кислот по реакции с реактивами Гриньяра и диоксидом углерода описано в разд. 19.1.
Бензойную кислоту можно получить окислением метильной боковой цепи метилбензола (см. разд. 18.2).
Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Каннищаро. В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенил-метанола:
Окисление

Реакция Канниццаро характерна для альдегидов, не имеющих -атомов водорода. Так называются атомы водорода, присоединенные к атому углерода, соседнему с альдегидной группой:

Поскольку метаналь не имеет -атомов водорода, он может вступать в реакцию Канниццаро. Альдегиды, содержащие по крайней мере один -атом водорода, в присутствии раствора гидроксида натрия подвергаются кислотнокатализируемой альдольной конденсации (см. выше).
Химические свойства
Хотя карбоксильная группа содержит карбонильную группу, карбоновые кислоты не вступают в некоторые реакции, характерные для альдегидов и кетонов. Например, они не вступают в реакции присоединения или конденсации. Это объясняется тем, что атом
углерода в карбоксильной группе имеет меньший положительный заряд, чем в альдегидной или кетогруппе.
Кислотность. Оттягивание электронной плотности от карбоксильного атома водорода ослабляет связь О-Н. Вследствие этого карбоксильная группа способна отщеплять (терять) протон. Поэтому монокарбоновые кислоты ведут себя как одноосновные кислоты. В водных растворах этих кислот устанавливается следующее равновесие:
Карбоксилат-ион может рассматриваться как гибрид двух резонансных структур:

Иначе его можно представлять себе как
Делокализация электрона между атомами карбоксилатной группы стабилизирует карбоксилат-ион. Поэтому карбоновые кислоты обладают намного большей кислотностью, чем спирты. Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие сильно сдвинуто влево. Таким образом, карбоновые кислоты - это слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой кислотности
Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта. Такие заместители, как хлор, оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, Они ослабляют карбоновую кислоту:

Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях для ряда кислот, указанных в табл. 19.12.
Таблица 19.12. Значения карбоновых кислот

Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они вступают в реакции с реакционноспособными металлами, основаниями, щелочами, карбонатами и гидрокарбонатами, образуя соответствующие соли (табл. 19.13). Реакции, указанные в этой таблице, характерны и для растворимых и нерастворимых карбоновых кислот.
Подобно другим солям слабых кислот, карбоксилатные соли (соли карбоновых кислот) реагируют с минеральными кислотами, взятыми в избыточном количестве, образуя исходные карбоновые кислоты. Например, при добавлении раствора гидроксида натрия к взвеси нерастворимой бензойной кислоты в воде происходит растворение кислоты вследствие образования бензоата натрия. Если затем к полученному раствору добавить серную кислоту, происходит осаждение бензойной кислоты:
Таблица 19.13. Образование солей из карбоновых кислот

Этерификация. При нагревании смеси карбоновой кислоты со спиртом в присутствии концентрированной минеральной кислоты происходит образование сложного эфира. Такой процесс, называемый этерификацией, требует расщепления молекул спирта. При этом существуют две возможности.
1. Алкоксиводородное расщепление. В данном случае спиртовый атом кислорода (из гидроксильной группы) попадает в молекулу образующегося эфира:
2. Алкилгидроксилъное расщепление. При расщеплении такого типа спиртовый атом кислорода попадает в молекулу воды:
Какой из этих случаев реализуется конкретно, можно определить экспериментально, проводя этерификацию с использованием спирта, содержащего изотоп 180 (см. разд. 1.3), т.е. с использованием изотопной метки. Определение относительной молекулярной массы образующегося эфира с помощью масс-спектрометрии показывает, присутствует ли в нем изотопная метка-кислород-18. Таким способом обнаружено, что этерификация с участием первичных спиртов приводит к образованию меченых сложных эфиров:

Это показывает, что молекула метанола в ходе рассматриваемой реакции подвергается метокси-водородному расщеплению.
Галогенирование. Карбоновые кислоты реагируют с пентахлоридом фосфора и оксид-дихлоридом серы, образуя хлорангидриды соответствующих кислот. Например

И бензоилхлорид, и оксид-трихлорид фосфора представляют собой жидкости, которые необходимо отделить друг от друга. Поэтому для хлорирования карбоновых кислот удобнее использовать оксид-дихлорид серы: это позволяет легко удалить газообразные хлороводород и диоксид серы из жидкого хлорангидрида карбоновой кислоты:
При продувании хлора через кипящую уксусную кислоту в присутствии таких катализаторов, как красный фосфор либо иод, и под действием солнечного света
образуется монохлороэтановая (монохлороуксусная) кислота:
Дальнейшее хлорирование приводит к образованию дизамешенного и тризамещенного продуктов:
Восстановление. При взаимодействии с лития в сухом диэтиловом эфире карбоновые кислоты могут восстанавливаться до соответствующих спиртов. Сначала образуется алкоксидное промежуточное соединение, гидролиз которого приводит к образованию спирта:
Карбоновые кислоты не восстанавливаются многими обычными восстановителями. Эти кислоты не могут восстанавливаться сразу до соответствующих альдегидов.
Окисление. За исключением метановой (муравьиной) и этановой (уксусной) кислот, остальные карбоновые кислоты окисляются с трудом. Муравьиная кислота и ее соли (формиаты) окисляются перманганатом калия. Муравьиная кислота способна восстанавливать реактив Фелинга и при нагревании в смеси с водно-аммиачным раствором нитрата серебра образует «серебряное зеркало». При окислении муравьиной кислоты образуются диоксид углерода и вода:
Этандиовая (щавелевая) кислота тоже окисляется перманганатом калия, образуя диоксид углерода и воду:

Дегидратация. Перегонка карбоновой кислоты с каким-либо обезвоживателем, например оксидом приводит к отщеплению молекулы воды от двух молекул кислоты и образованию ангидрида карбоновой кислоты:

Муравьиная и щавелевая кислоты оказываются исключениями и в этом случае. Дегидратация муравьиной кислоты или ее калиевой либо натриевой соли с помощью концентрированной серной кислоты приводит к образованию моноксида углерода и
Дегидратация метаноата (формиата) натрия концентрированной серной кислотой представляет собой обычный лабораторный способ получения моноксида углерода. Дегидратация щавелевой кислоты горячей концентрированной серной кислотой приводит к образованию смеси моноксида углерода и диоксида углерода:

Карбоксилаты
Натриевые и калиевые соли карбоновых кислот представляют собой кристаллические вещества белого цвета. Они легко растворяются в воде, образуя сильные электролиты.
Электролиз натриевых или калиевых карбоксилатных солей, растворенных в водно-метанольной смеси, приводит к образованию алканов и диоксида углерода на аноде и водорода на катоде.
На аноде:
На катоде:
Такой метод получения алканов называется электрохимическим синтезом Кольбе.
Образование алканов происходит и при нагревании смеси карбоксилатов натрия или калия с гидроксидом натрия либо натронной известью. (Натронная известь - это смесь гидроксида натрия с гидроксидом кальция.) Такой способ используется, например, для получения метана в лабораторных условиях:

Ароматические карбоксилаты натрия или калия в аналогичных условиях образуют арены:

При нагревании смеси карбоксилатов натрия с хлорангидридами образуются ангидриды соответствующих карбоновых кислот:

Карбоксилаты кальция тоже представляют собой кристаллические вещества белого цвета и, как правило, растворимы в воде. При их нагревании происходит образование
ние с низким выходом соответствующих кетонов:

При нагревании смеси карбоксилатов кальция с формиатом кальция образуется альдегид:

Аммониевые соли карбоновых кислот тоже представляют собой белые кристаллические вещества, растворимые в воде. При сильном нагревании они образуют соответствующие амиды: